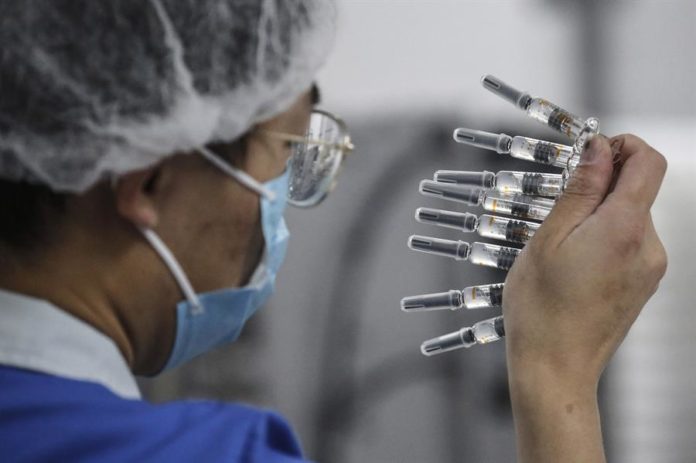
En tiempo récord surge primera vacuna contra el COVID-19
Norristown, PA – El año está por concluir y, de la misma forma, muchos esperamos que este 2020 se vaya junto con la pesadilla de la pandemia. Podríamos decir que, con la reciente aprobación de la primera vacuna contra el coronavirus SARS-CoV-2, el fin de la peste se vislumbra cerca; sin embargo, debemos conservar la calma; la cura del COVID-19 y el regreso a la normalidad aún está muy lejos de ocurrir. Sin la intención de desalentar a la población, es importante dimensionar y no perder de vista el camino que ha recorrido la vacuna, y lo que falta por recorrer.
La vacuna BNT162 de Pfizer/BioNTech es de tipo ARNm; esto significa que el material genético de la vacuna se encuentra envuelto en una capa de nanopartículas de grasa que, para mantenerlo viable, es necesario conservarlo a una temperatura de -94°F (-70°C); lo cual requiere de equipo especial para su transporte. Es una vacuna que consta de dos dosis, las cuales se aplicarán con un espacio de tres o cuatro semanas entre una y otra, ofreciendo hasta un 95% de efectividad contra el coronavirus SARS-CoV-2. En la fase 3 del estudio, solo el 0.02% del total de los voluntarios que recibieron la vacuna adquirieron el coronavirus. Esta es la primera vacuna fabricada en tiempo récord; su desarrollo se produjo en tan sólo 10 meses, siguiendo los mismos pasos que normalmente requieren hasta 10 años.
Antes de que cualquier vacuna se pueda aplicar a la población, primero tiene que ser autorizada por la agencia de salud del país en cuestión. En el mundo existen muchas agencias; entre las más prestigiosas se encuentran la Administración de Medicamentos y Alimentos de los EE. UU., FDA (Food & Drug Administration); la Agencia Europea de Medicamentos, EMA (European Medicines Agency), y la británica Agencia Reguladora de Medicamentos y Productos Sanitarios. MHRA (Medicines and Healthcare products Regulatory Agency); la cual, el pasado 2 de diciembre dio la aprobación a Pfizer/BioNTech para usar la primera vacuna contra el COVID-19 en el Reino Unido.
La decisión de la autoridad reguladora de la Gran Bretaña se tomó con el asesoramiento de la Comisión de Medicamentos Humanos, CHM (Commission on Human Medicines), organismo asesor científico experto, independiente del gobierno. Un equipo de académicos y médicos expertos del MHRA llevó a cabo una revisión rigurosa, científica y detallada de todos los datos disponibles desde octubre de 2020, los cuales involucraron estudios preclínicos de laboratorio, ensayos clínicos, controles de fabricación y calidad, muestreo del producto, pruebas de la vacuna final, y las condiciones para asegurar su suministro y distribución.
Al respecto, el Instituto Nacional de Estándares y Controles Biológicos, parte de la agencia MHRA, ha estado y seguirá haciendo pruebas de laboratorio independientes para que cada lote de la vacuna cumpla con los estándares esperados de seguridad y calidad.
Las primeras 800,000 dosis estuvieron disponibles en el Reino Unido a partir de la segunda semana de diciembre, informó Matt Hancock, ministro de Salud Británico; es decir, por ahora 400,000 personas recibenn el esquema de vacunación completo, en el que se da prioridad a adultos mayores, residentes de asilos y personal sanitario. De acuerdo con el Banco Mundial, en 2019 el Reino Unido contaba con una población de 66,834,400 habitantes, lo que significa que, en esta primera entrega, aproximadamente el 0.6% de la gente será vacunada.
Actualmente, un total de 172 países y múltiples vacunas candidatas se encuentran en conversaciones sobre una posible participación en el COVAX (Acelerador del acceso a las herramientas contra la COVID-19); una iniciativa mundial destinada a colaborar con los fabricantes de vacunas, de modo que los países de todo el mundo tengan un acceso equitativo a vacunas seguras y eficaces una vez que estas hayan obtenido la licencia y la autorización, (Organización Mundial de la Salud). Varias vacunas candidatas se encuentran ya en fase 3, por ejemplo, la mRNA-1273 de Moderna; AZD1222 del consorcio Universidad de Oxford, Astra Zeneca, IQVIA e Instituto Serum de India; la Ad5-nCoV de CanSino Biologics; CoronaVac, de Sinovac; Covaxin, de Bharat Biotech y el Instituto Nacional de Virología; Ad26.COV2.S de Johnson & Johnson y la NVX-CoV2373 de Novavax.
Finalmente, debemos tranquilizarnos, puesto que hasta que al menos el 80% de la población no se encuentre vacunada y se genere la “Inmunidad de rebaño”, no disminuirá el riesgo de contagio; por lo que aún es imprescindible continuar con las medidas recomendadas para salvaguardar nuestra salud: uso de mascarilla, ejercer la distancia social, lavado de manos, usar gel antibacterial (de alcohol al 70%) y evitar reuniones numerosas.